Jenis-Jenis Senyawa Asam,Basa, Dan Garam Beserta Contohnya ( Part II )
3. Basa Kuat
Sama halnya dengan asam kuat, basa kuat ini dapat terionisasi 100 % membentuk ion-ion. Karena senyawa basa kuat ini dapat terionisasi sempurna di dalam air, maka senyawa basa kuat ini dapat digolongkan ke dalam jenis senyawa elektrolit kuat.Contohnya : Ba(OH)2 → Ba2+ + 2OH-
Barium Hidroksida diatas terionisasi sempurna membentuk ion Ba2+ dan ion 2OH- . Basa kuat dikategorikan sebagai senyawa elektrolit kuat dan ia juga memiliki daya ionisasi yang cukup kuat.
Baiklah ini beberapa contoh senyawa basa kuat yang umum kita ketahui :
1. Natrium Hidroksida ( NaOH )
2. Lithium Hidroksida ( LiOH )
3. Kalium Hidroksida ( KOH )
4. Rubidium Hidroksida ( RbOH )
5. Kalsium Hidroksida ( Ca(OH)2 )
6. Strontium Hidroksida ( Sr(OH)2 )
7. Barium Hidroksida ( Ba(OH)2 )
Ok, itulah penjelasan dan contoh mengenai senyawa basa kuat, sekarang kita lanjutkan ke penjelasan dan contoh mengenai senyawa basa lemah.
4. Basa Lemah
Basa lemah merupakan basa yang hanya dapat terionisasi sebagian membentuk ion-ion, karena hanya sebagian saja molekulnya yang berubah menjadi ion-ion, maka senyawa basa lemah ini hanya dapat dikategorikan sebagai senyawa elektrolit lemah, bukan sebagai senyawa elektrolit kuat.Contohnya : NH3 ⇄ NH4+ + OH-
Amonium Hidroksida diatas terionisasi sebagian membentuk ion ammonium ( NH4+ ) dan ion hidroksida ( OH- ). Basa lemah dikategorikan sebagai senyawa elektrolit lemah dan ia juga memiliki daya ionisasi yang lemah.
Berikut ini beberapa contoh senyawa basa lemah yang umum kita ketahui :
1. Ammonium Hidroksida ( NH4OH )
2. Hidrazin ( NH2NH2 )
3. Alumunium Hidroksida ( Al(OH)3 )
4. Tembaga(II)Hidroksida ( Cu(OH)2 )
5. Besi(II)Hidroksida ( Fe(OH)2 )
6. Nikel(II)Hidroksida ( Ni(OH)2 )
7. Magnesium Hidroksida ( Mg(OH)2 )
8. Berilium Hidroksida ( Be(OH)2 )
Ok, itulah penjelasan dan contoh mengenai senyawa basa lemah, sekarang mari kita lanjutkan ke penjelasan dan contoh mengenai garam yang bersifat netral !
5. Garam Yang Bersifat Netral
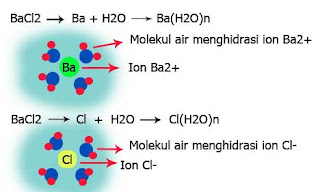
Garam yang bersifat netral merupakan garam yang dihasilkan dari reaksi antara asam kuat dan basa kuat serta juga dapat dihasilkan dari reaksi antara asam lemah dengan basa lemah yang memiliki kesaman nilai Ka dan Kb. Ketika garam tersebut dilarutkan ke dalam air, maka garam tersebut akan terhidrasi sederhana bersama molekul-molekul air.Berikut ini contoh dan ilustrasi gambarnya :
BaCl2 → Ba2+ + 2Cl-
( Garam BaCl2 merupakan garam yang bersifat netral yang dihasilkan dari asam kuat dan basa kuat )
Karena garam tersebut tidak bereaksi dengan molekul air, melainkan hanya terhidrasi sederhana, maka larutan garam yang dihasilkan akan bersifat netral.
Berikut ini contoh dari senyawa garam yang bersifat netral :
1. Lithium Klorida ( LiCl ) 6. Barium Klorida ( BaCl2 )
2. Natrium Klorida ( NaCl ) 7. Kalium Bromida ( KBr )
3. Kalium Klorida ( KCl ) 8. Natrium Bromida ( NaBr )
4. Rubidium Klorida ( RbCl ) 9. Kalsium Bromida ( CaBr2 )
5. Kalsium Klorida ( CaCl2 ) 10. Kalium Nitrat ( KNO3 )
11. Natrium Nitrat ( NaNO3 )
12. Kalium Sulfat ( K2SO4 )
13. Natrium Perklorat ( NaClO4 )
14. Kalium Iodida ( KI )
15. Kalium Permanganat ( KMnO4 ) dan masih banyak lagi !!
Baiklah itulah penjelasan dan contoh mengenai senyawa garam yang bersifat netral, sekarang mari kita lanjutkan ke penjelasan dan contoh mengenai senyawa garam yang bersifat asam !
Selanjutnya >>
1 comment for "Jenis-Jenis Senyawa Asam,Basa, Dan Garam Beserta Contohnya ( Part II )"
Apakah Sobat Masih Bingung ? Jangan Malu-Malu Sampaikan Saja Keluh Kesah Sobat Di Kolom Komentar !