Panduan : Pengertian Pereaksi Pembatas Serta Cara Menentukan Pereaksi Pembatas
Hello Sobat!! Salam Chemistry !!
Pada panduan kali ini, kita akan belajar bagaimana caranya menentukan pereaksi pembatas. Sebelumnya, kita telah membahas konsep mol dan kita juga telah mempelajari bagaimana cara menentukan mol dari suatu unsur/senyawa dengan menggunakan perbandingan koofesien reaksi pada suatu reaksi kimia.
Nah, untuk menentukan pereaksi pembatas maka kedua konsep diatas sangatlah diperlukan, karena dengan mengetahui mol masing-masing unsur/senyawa pada suatu reaksi kimia, maka kita dapat menentukan unsur mana yang habis bereaksi dan unsur mana yang tidak habis bereaksi.
oke , sebelum kita bahas lebih dalam, sekarang marilah kita bahas dulu mengenai pengertian dari pereaksi pembatas. Pereaksi pembatas ialah suatu unsur/senyawa yang habis bereaksi dengan unsur/senyawa lain untuk membentuk suatu produk.
Analoginya begini :
Misalkan terjadi reaksi kimia antara unsur A dengan unsur B membentuk senyawa AB seperti ditunjukkan pada reaksi dibawah ini :
A + B → AB
Ternyata saat reaksi selesai, unsur A masih tersisa sebanyak 5 gr ( tidak habis bereaksi ) sedangkan unsur B habis bereaksi ( tidak bersisa ) , maka dalam hal ini yang bertindak sebagai pereaksi pembatas ialah unsur B!
Jadi berdasarkan analogi diatas dapat kita simpulkan bahwa pereaksi pembatas ialah suatu unsur/senyawa yang habis bereaksi dengan unsur/senyawa lain untuk membentuk suatu produk.
Sekarang coba sobat perhatikan persamaan reaksi kimia di bawah ini :
1. Zn + 2 HCl → ZnCl2 + H2
1 : 2 : 1 : 1
2. N2 + 3 H2 → 2 NH3
1 : 3 : 2
3. CH4 + 2 O2 → CO2 + 2 H2O
1 : 2 : 1 : 2
Ketiga reaksi kimia diatas masing-masing memiliki perbandingan koofesien reaksi, namun tahukah sobat arti dari perbandingan koofesien reaksi diatas ? kita ambil contoh reaksi pertama, Zn dan HCl memiliki perbandingan koofesien reaksi 1 : 2 , artinya 1 mol Zn akan habis bereaksi dengan 2 mol HCl begitu juga sebaliknya 2 mol HCl akan habis bereaksi dengan 1 mol Zn. Bagaimana jika 2 mol Zn direaksikan dengan 4 mol HCl , apakah Zn akan habis bereaksi dengan HCl ? ya tentu , selain perbandingan mol nya sama dengan perbandingan koofeseienya yaitu 1 : 2 maka kedua reaktan ( Zn dan HCl ) akan habis bereaksi.
Sekarang kita masuk ke contoh soal yang berkaitan dengan materi pereaksi pembatas, silahkan disimak !
1. Direaksikan 1 mol Zn dengan 0,5 Mol HCl sesuai dengan persamaan reaksi berikut.
Zn + 2 HCl → ZnCl2 + H2 ( Sudah Setara )
1 : 2
Tentukanlah pereaksi pembatasnya !
Jawab : Diketahui perbandingan jumlah mol Zn dan HCl yang direaksikan ialah 1 : 0,5 atau sama dengan 2 : 1, maka untuk mencari pereaksi pembatasnya kita dapat gunakan 2 cara.
Cara pertama, kita dapat gunakan perbandingan koofesien untuk menentukan pereaksi pembatasnya, telah kita ketahui bahwa perbandingan koofesien Zn dan HCl pada persamaan reaksi diatas ialah 1 : 2, yang artinya 1 mol Zn akan habis bereaksi dengan 2 mol HCl atau 2 mol Zn akan habis bereaksi dengan 4 mol HCl dan seterusnya asal perbandingan jumlah molnya sesuai dengan perbandingan koofesienya yaitu 1 : 2, sementara pada soal diketahui jumlah mol HCl yang bereaksi hanya 0,5 mol , Artinya ?
Artinya, HCl lah yang bertindak sebagai pereaksi pembatas karena untuk menghabiskan 1 mol Zn diperlukan 2 mol HCl ( sesuai dengan perbandingan koofesien 1 : 2 ), sementara hanya tersedia 0,5 mol HCl, jadi dapat disimpulkan bahwa HCl akan habis bereaksi sedangkan logam Zn akan bersisa di akhir reaksi.
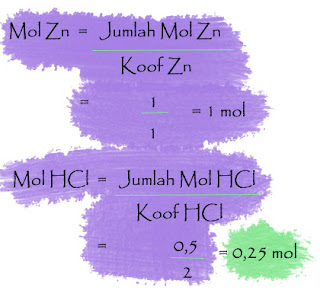
Cara kedua, kita dapat cari pereaksi pembatasnya dengan cara membagi jumlah mol masing-masing reaktan dengan koofesienya, cara seperti ini lazim saya sebut dengan cara konsep mol :
Karena HCl memiliki mol yang paling kecil maka HCl lah yang bertindak sebagai pereaksi pembatas dan akan habis saat reaksi selesai sedangkan Zn akan bersisa di akhir reaksi.
gimana sob ? sampai disini sudah mulai paham ? jika iya mari kita lanjut ke contoh soal no 2..
2. Direaksikan 2 mol gas N2 dengan 5 mol gas H2 sesuai dengan persamaan reaksi berikut ini.
N2 + 3 H2 → 2 NH3 ( Sudah Setara )
1 : 3
Tentukanlah pereaksi pembatasnya !
Pada soal diatas diketahui perbandingan jumlah mol reaktan yang direaksikan ialah 2 : 5, sedangkan perbandingan koofesien N2 dan H2 ialah 1 : 3, dalam hal ini, maka dapat dipastikan H2 lah yang bertindak sebagai pereaksi pembatas, karena untuk menghabiskan 2 mol N2 maka dibutuhkan 6 mol H2 ( sesuai dengan perbandingan koofesien 1 : 3 ), sementara hanya tersedia 5 mol H2, jadi dapat disimpulkan bahwa H2 akan habis bereaksi, sedangkan N2 akan bersisa di akhir reaksi.
Sekarang kita cari dengan cara konsep mol yaitu dengan cara membagi jumlah mol masing-masing reaktan dengan koofesienya.
3. Direaksikan 1 mol SO2 dengan 1 mol O2 sesuai dengan persamaan reaksi berikut ini.
2 SO2 + O2 → 2 SO3 ( Sudah Setara )
2 : 1
Maka tentukanlah :
a. Pereaksi Pembatas
b. Banyak mol zat sisa
c. Banyak mol gas SO3 yang dihasilkan
A. Jawab ( menentukan pereaksi pembatas )
Dari soal diketahui perbandingan koofesien dari SO2 dan O2 yaitu 2 : 1 dan perbandingan jumlah mol reaktan yang direaksikan ialah 1 : 1 , sekarang kita cari pereaksi pembatasnya dengan cara melihat perbandingan koofesienya terlebih dahulu, perbandingan koofesien dari reaksi diatas ialah 2 : 1 yang artinya untuk menghabiskan 1 mol O2 maka diperlukan 2 mol SO2 ( Sesuai dengan perbandingan koofesien 2 : 1 ), sementara hanya tersedia 1 mol SO2, artinya SO2 akan habis bereaksi di akhir reaksi , so dapat dipastikan pereaksi pembatasnya ialah SO 2.
Ok sekarang kita cari pereaksi pembatasnya dengan cara menggunakan konsep mol….
B. Sedangkan jumlah mol zat sisa dapat dengan mudah kita cari dengan cara mengurangkan kedua mol reaktan diatas
Banyak mol zat sisa = 1 – 0,5 = 0,5 mol O2
Jadi O2 bertindak sebagai sisa hasil reaksi.
C. Jumlah mol SO3 yang dihasilkan dapat kita cari dengan menggunakan rumus :
Zn + 2 HCl → ZnCl2 + H2 ( Sudah Setara ) ( STP )
Maka tentukanlah :
A. Pereaksi pembatas
B. Banyak mol zat sisa
C. Volume gas H2 yang dihasilkan
Jawab A : Sebelum menenetukan pereaksi pembatasnya, alangkah baiknya kita cari jumlah mol dari logam Zn dan HCl nya terlebih dahulu…
Jumlah mol Zn = gr/Mr = 130/65 = 2 Mol
Jumlah mol HCl = M x V = 3 x 1 = 3 Mol
Setelah itu barulah kita cari pereaksi pembatasnya dengan cara menggunakan konsep mol .
B. Banyak Mol Zat Sisa
= 2 – 1,5 = 0,5 mol Zn, jadi saat reaksi selesai, Zn masih tersisa sebanyak 0,5 mol.
C. Volume Gas H2 Yang Dihasilkan
Untuk mencari volume suatu gas dalam keadaan STP, maka digunakan rumus :
V = n x 22,4 L
Maka pertama kita cari mol nya terlebih dahulu dengan cara :
Sehingga Volumenya = 1,5 x 22,4 L = 33,6 L Gas H
5. Direaksikan 4 mol gas etilen (C2H2) dengan 8 mol gas O2 dalam wadah tertutup sesuai dengan persamaan reaksi berikut ini.
2 C2H2 + 5 O2 → 4 CO2 + 2 H2O ( Sudah Setara ) ( STP )
Maka tentukanlah :
A. Pereaksi Pembatas
B. Banyak Mol Zat Sisa
C. Mol CO2 dan H2O Yang Dihasilkan
Jawab A ( Menetukan Pereaksi Pembatas )
Kita cari pereaksi pembatasnya dengan cara konsep mol
Mol C2H2 = Jumlah Mol C2H2 / Koof C2H2
= 4/2 = 2 Mol
Mol O2 = Jumlah Mol O2 / Koof O2
= 8/5 = 1,6 Mol
B. Banyak Mol Zat Sisa
2 – 1,6 = 0,4 mol C2H2
C. Mol CO2 dan H2O yang dihasilkan dapat dicari dengan menggunakan rumus :
Nah, bagaimana Sob ? sudah pahamkan materi mengenai pereaksi pembatas ini ? Mmm terus terang sobat, dulu saat saya masih kelas 1 SMA, saya paling tidak suka belajar materi mengenai pereaksi pembatas ini, karena saya tidak mengerti sama sekali cara menentukan pereaksi pembatasnya, usut punya usut ternyata penyebab saya tidak mengerti karena saya tidak menguasai cara menentukan mol unsur/senyawanya, so apa boleh buat nilai ulangan saya menjadi rendah hehehe… ( aduhh le.. le.. nilai ulangan rendah kok malah ketawa…sampean dah gila..? hahaha )
Tetapi semenjak kejadian itu, saya taubat dan terus berusaha belajar bagaimana caranya menentukan mol dan dengan kesungguhan saya untuk mempelajari konsep mol tersebut pada akhirnya saya jadi mudah untuk menentukan pereaksi pembatasnya walaupun materi pereaksi pembatas sudah saya lewati waktu itu.
Dan saya memutuskan untuk membagikan ilmu yang saya dapat untuk sobat semua agar sobat bisa terbantu dan lebih paham cara menentukan pereaksi pembatas dan semoga saja sobat mendapat nilai ulangan yang lebih tinggi dari saya hehehe ( aminnn )…
Oke deh, apabila sobat masih bingung atau punya pertanyaan sobat bisa berkomentar di akhir artikel ini,, terima kasih dan salam Chemistry !!






2 comments for "Panduan : Pengertian Pereaksi Pembatas Serta Cara Menentukan Pereaksi Pembatas"
Apakah Sobat Masih Bingung ? Jangan Malu-Malu Sampaikan Saja Keluh Kesah Sobat Di Kolom Komentar !