Struktur Dan Sifat Air
Air merupakan senyawa kimia yang paling umum dan paling sering kita jumpai dalam kehidupan kita sehari-hari. Semua keseharian kita selalu tidak pernah lepas dari air, mulai dari kita bangun tidur sampai kita tidur lagi, rasanya tak mungkin kita tidak menyentuh air. Intinya, semua kehidupan keseharian kita tak pernah lepas dari si air. Meskipun begitu, tak banyak orang yang tahu mengenai sifat-sifat dan keunikan yang dimiliki oleh air, Maka pada postingan kali ini, marilah kita ulik beberapa sifat-sifat unik yang dimiliki oleh Air !
Air merupakan pelarut yang sangat baik bagi senyawa ion dan berbagai zat lain yang mampu membentuk ikatan hidrogen dengan air. Air memiliki kalor jenis yang tinggi, hal ini dikarenakan kuatnya ikatan hidrogen yang mengikat antara molekul air yang satu dengan molekul air yang lainya sehingga akan sangat sulit untuk memutuskan ikatan hidrogen tersebut. Dikarenakan tingginya kalor jenis yang dimiliki oleh air, maka air dapat menyerap kalor dalam jumlah cukup besar. Dan juga, air juga dapat melepaskan kalor dalam jumlah yang cukup besar. Dengan kemampuan uniknya ini, air dapat menjaga iklim di daratan sekitarnya dengan cara menyerap kalor pada musim panas dan melepaskan kalor pada musim dingin.
Salah satu keunikan yang dimiliki oleh air ialah sifat kerapatanya yang justru lebih rapat pada fase cair dibandingkan pada fase padat. Biasanya senyawa-senyawa kimia itu memiliki kerapatan yang lebih besar pada fase padat, tetapi hal itu tidak berlaku bagi air. Sifat uniknya ini dapat kamu amati ketika air membentuk es, coba saja celupkan es ke dalam air, es tersebut pasti terapung dan tidak tenggelam. Hal ini terjadi karena kerapatan air berkurang pada fase es, sehingga ia akan terapung di dalam air.
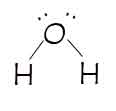
Salah satu sifat fisik yang dimiliki oleh air dan tidak dimiliki oleh senyawa kimia lainya ialah jumlah ikatan hidrogenya, Coba kamu tinjau bagaimana struktur molekul air, bila diperhatikan ternyata air memiliki 2 ikatan hidrogen yang mana senyawa kimia lain yang dapat membentuk ikatan hidrogen seperti NH3 dan HF hanya memiliki 1 ikatan hidrogen. Jadi ini benar-benar sangat unik dan hal itu membuat sifat-sifat yang dimiliki oleh air berbeda dari senyawa kimia lainya.
Di saat air berada dalam fase es atau padat, molekul-molekul air akan membentuk struktur 3 dimensi yang sangat teratur, yang mana hal ini dilakukan untuk mencegah molekul-molekul untuk terlalu dekat satu sama lain. Tetapi coba kamu bayangkan apa yang akan terjadi bila es meleleh ? Pada titik leleh, sejumlah molekul air mempunyai cukup energi kinetik untuk membebaskan diri dari ikatan hidrogen antarmolekul. Akibatnya, molekul-molekul ini menjadi terperangkap dalam rongga -ronga struktur 3 dimensi, yang terpecah-pecah menjadi kumpulan-kumpulan yang lebih kecil. Hasilnya, lebih banyak molekul per satuan volume dalam air cair daripada dalam es. Jadi, karena kerapatan merupakan massa dibagi volume, maka kerapatan air menjadi lebih besar daripada kerapatan es. Dengan pemanasan lebih lanjut, lebih banyak molekul air yang akan lepas dari ikatan hidrogen antar molekul sehingga pada rentang suhu 0-4 C , air akan semakin rapat. Suhu 4 C merupakan suhu dimana air berada pada kerapatan terbesarnya. Tetapi pada suhu diatas 4 C, air akan mengalami pemuaian termal dan kerapatanya akan semakin berkurang.
Air merupakan pelarut yang sangat baik bagi senyawa ion dan berbagai zat lain yang mampu membentuk ikatan hidrogen dengan air. Air memiliki kalor jenis yang tinggi, hal ini dikarenakan kuatnya ikatan hidrogen yang mengikat antara molekul air yang satu dengan molekul air yang lainya sehingga akan sangat sulit untuk memutuskan ikatan hidrogen tersebut. Dikarenakan tingginya kalor jenis yang dimiliki oleh air, maka air dapat menyerap kalor dalam jumlah cukup besar. Dan juga, air juga dapat melepaskan kalor dalam jumlah yang cukup besar. Dengan kemampuan uniknya ini, air dapat menjaga iklim di daratan sekitarnya dengan cara menyerap kalor pada musim panas dan melepaskan kalor pada musim dingin.
Salah satu keunikan yang dimiliki oleh air ialah sifat kerapatanya yang justru lebih rapat pada fase cair dibandingkan pada fase padat. Biasanya senyawa-senyawa kimia itu memiliki kerapatan yang lebih besar pada fase padat, tetapi hal itu tidak berlaku bagi air. Sifat uniknya ini dapat kamu amati ketika air membentuk es, coba saja celupkan es ke dalam air, es tersebut pasti terapung dan tidak tenggelam. Hal ini terjadi karena kerapatan air berkurang pada fase es, sehingga ia akan terapung di dalam air.
Salah satu sifat fisik yang dimiliki oleh air dan tidak dimiliki oleh senyawa kimia lainya ialah jumlah ikatan hidrogenya, Coba kamu tinjau bagaimana struktur molekul air, bila diperhatikan ternyata air memiliki 2 ikatan hidrogen yang mana senyawa kimia lain yang dapat membentuk ikatan hidrogen seperti NH3 dan HF hanya memiliki 1 ikatan hidrogen. Jadi ini benar-benar sangat unik dan hal itu membuat sifat-sifat yang dimiliki oleh air berbeda dari senyawa kimia lainya.
Di saat air berada dalam fase es atau padat, molekul-molekul air akan membentuk struktur 3 dimensi yang sangat teratur, yang mana hal ini dilakukan untuk mencegah molekul-molekul untuk terlalu dekat satu sama lain. Tetapi coba kamu bayangkan apa yang akan terjadi bila es meleleh ? Pada titik leleh, sejumlah molekul air mempunyai cukup energi kinetik untuk membebaskan diri dari ikatan hidrogen antarmolekul. Akibatnya, molekul-molekul ini menjadi terperangkap dalam rongga -ronga struktur 3 dimensi, yang terpecah-pecah menjadi kumpulan-kumpulan yang lebih kecil. Hasilnya, lebih banyak molekul per satuan volume dalam air cair daripada dalam es. Jadi, karena kerapatan merupakan massa dibagi volume, maka kerapatan air menjadi lebih besar daripada kerapatan es. Dengan pemanasan lebih lanjut, lebih banyak molekul air yang akan lepas dari ikatan hidrogen antar molekul sehingga pada rentang suhu 0-4 C , air akan semakin rapat. Suhu 4 C merupakan suhu dimana air berada pada kerapatan terbesarnya. Tetapi pada suhu diatas 4 C, air akan mengalami pemuaian termal dan kerapatanya akan semakin berkurang.

Post a Comment for "Struktur Dan Sifat Air"
Apakah Sobat Masih Bingung ? Jangan Malu-Malu Sampaikan Saja Keluh Kesah Sobat Di Kolom Komentar !